総括報告書
研究責任医師(多施設共同研究の場合には代表医師)は、全ての評価項目に係るデータの収集を行うための期間が終了してから原則1年以内に総括報告書を提出しなければいけません。
総括報告書に含むべき事項
- 臨床研究の対象者の背景情報(年齢、性別等)
- 臨床研究のデザインに応じた進行状況に関する情報(対象者数の推移等)
- 疾病等の発生状況のまとめ
- 主要評価項目及び副次評価項目のデータ解析及び結果
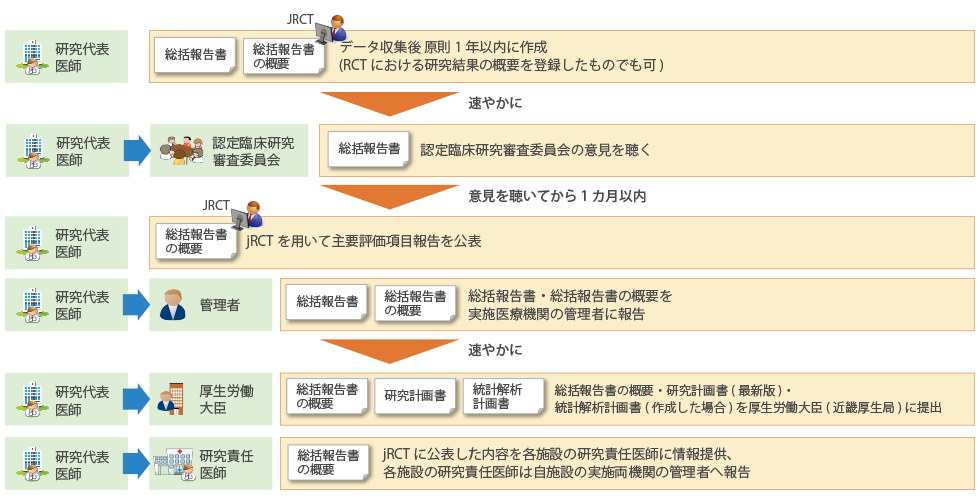
総括報告書の書式
提出書類
| 様式 | 備考 | |
|---|---|---|
| 1 | 終了通知書 | 記載上の留意事項については、記載方法 参照 |
| 2 | 総括報告書 | 少なくとも以下の事項を含めて記載してください。
|
| 3 | 終了届書(総括報告書の概要) |